Esse texto foi escrito por Phillipe Pereira Travassos, CRM SP 188775, Médico intensivista, diarista do grupo PacienteGraveUTI
DEFINIÇÃO E EPIDEMIOLOGIA
Hemorragia subaracnoide (HSA) é o preenchimento do espaço subaracnóideo por sangue proveniente da ruptura de um aneurisma cerebral
80% das HSA não traumáticas são secundárias a aneurisma e das HSA não aneurismáticas podemos ter:
HSA perimesencefálica – Geralmente, são menores e têm melhor prognóstico
HSA pretruncal secundária a hematoma intramural de a. basilar
A incidência é de 6 a 10 casos a cada 100 mil habitantes na população mundial ao ano
Corresponde de 5 a 10% de todos os AVCs
Mortalidade de 25 a 50% e sequelas podem chegam a 50%.
Idade média: 50 anos, ou seja, população em idade produtiva
É mais comum em mulheres na quinta ou sexta década de vida e está associada a hipertensão, tabagismo, abuso de álcool e uso de drogas simpaticomiméticas (e.g. cocaína)
A principal causa de morte não é cerebral, e sim cardíaca (58%)
Até 46% dos pacientes que sobrevivem apresentam déficit cognitivo a longo prazo, com prejuízo da funcionalidade e da qualidade de vida
Principais artérias acometidas:
Comunicante Posterior (25%)
Comunicante Anterior (30%)
Cerebral Média (20%)
FATORES DE RISCO
Fatores de risco não modificáveis são:
Parente de primeiro grau com HSA aneurismática
Displasia fibromuscular
Doença renal policística
Síndrome de Ehler-Danlos (tipo IV)
CLÍNICA
A cefaleia é o principal achado da HSA e pode ser sintoma isolado em 40% dos casos
80% dos pacientes descrevem como a pior cefaleia da vida
Thunderclap headache: (‘’cefaleia em trovoadas’’). Tem início súbito e atinge a máxima intensidade em poucos segundos
A cefaleia sentinela (cefaleia que precede a ruptura do aneurisma em uma a duas semanas) é relatada em até 40% das HSAs e ocorrem devido a pequenas expansões do aneurisma, ou a pequenas hemorragias. Nesse contexto, se conseguirmos diagnosticar HSA nessa fase, o prognóstico será muito melhor.
Outros sintomas incluem náuseas, vômitos, rigidez de nuca, fotofobia, rebaixamento do nível de consciência e sinal neurológico focal
A ruptura pode ser precipitada por esforço físico intenso
Fundo de olho deve ser realizado em todos os pacientes, em busca de hemorragias retinianas, podendo ser o único achado no exame físico de pacientes inconscientes
Os sinais neurológicos focais mais comuns são:
Paralisia do III nervo craniano (aneurisma de comunicante posterior)
Paralisia do VI nervo craniano (devido a aumento da pressão intracraniana)
Paresia de ambos os membros inferiores (aneurisma de comunicante anterior)
Hemiparesia, afasia e heminegligência (aneurisma de artéria cerebral média)
DIAGNÓSTICO POR IMAGEM E DIFERENCIAL


A principal escala utilizada é a Escala de Fisher Modificado
Na verdade, a Escala de Fisher não é uma escala prognóstica. Ela prediz o risco de vasoespasmo cerebral. A hemorragia ventricular é o principal preditor de vasoespasmo e, por isso, a escala foi modificada. Na escala antiga, o Grau III tinha maior risco de vasoespasmo do que o grau IV.
A tomografia computadorizada (TC) sem contraste é o exame de escolha para o paciente que chega ao pronto socorro com cefaleia súbita e de forte intensidade, chegando a ter sensibilidade próxima a 95% nos primeiros 3 dias
Uma tomografia normal, não exclui HSA
A sensibilidade da TC é reduzida substancialmente após esse período, sendo necessária a realização da punção lombar para demonstrar xantocromia
A punção deve ser realizada em pacientes com suspeita de HSA e TC negativa
Devem ser colhidos 4 tubos consecutivos e enviados para análise
A não redução da contagem de hemácias do primeiro ao quarto tubo é sugestivo de HSA
Após 12 horas do episódio já é possível perceber xantocromia e essa é suficiente para o diagnóstico
Pressão de abertura elevada também é sugestiva de HSA
O diagnóstico diferencial abrange:
Outras formas de hemorragia como hematoma intraparenquimatoso, epidural e subdural
Outras causas de cefaleia como enxaqueca e tensional
Causa infecciosas: Meningoencefalites virais ou bacterianas
Caso o paciente apresente HSA identificável na TC ou líquor sugestivo ou duvidoso, deve-se proceder a angiotomografia (angio-TC) para pesquisa da causa da hemorragia
Caso a Angio-TC seja negativa, deve-se realizar angiografia
Eis as 2 principais escalas clínicas validadas para determinar gravidade dos pacientes com HSA:
World Federation of Neurological Surgeons (WFNS) – Leva em consideração a escala de Glasgow e a presença ou não de déficits neurológicos

Hunt and Hess Scale (H&H) – Leva em consideração a intensidade da inflamação meníngea, do déficit neurológico e o nível de consciência.

Tratamento
Os objetivos do tratamento são:
Prevenção do ressangramento. Clipagem cirúrgica ou embolização endovascular deve ser feita o quanto antes, preferencialmente, dentro das primeiras 24 horas e o risco maior de ressangramento esstá nas primeiras 6 horas
Manejo do vasoespasmo sintomático e isquemia cerebral tardia
Manejo de outras complicações neurológicas e suporte clínico intensivo
Tratamento medicamentoso
O controle pressórico deve ser feito com droga titulável (Ex. Nitroprussiato)
Para isso leva-se em consideração o risco de isquemia, ressangramento relacionado a pico hipertensivo e manutenção da pressão de perfusão cerebral (recomendação I, evidência A)
Não existe consenso para meta pressórica no aneurisma não tratado, porém manter a PAS < 160 mmHg é uma meta razoável
Nimodipino oral deve ser ofertado para todos os pacientes na dose de 60mg 4/4h, tendo sido demonstrada redução de mortalidade e de dependência (recomendação I, evidência A). Se o paciente apresentar hipotensão arterial, pode-se dividir a dose para 30mg 2/2h.
Apesar de não reduzir vasoespasmo, demonstrou melhorar desfechos neurológicos
Deve ser mantido por 14 a 21 dias
Não deve ser dado por via parenteral (relacionado a aumento da mortalidade)
Tratamento cirúrgico
Deve-se realizar a clipagem cirúrgica ou abordagem endovascular do aneurisma o quanto antes, a fim de reduzir o risco de ressangramento
A abordagem endovascular deve ser considerada para pacientes que possam ser submetidos a ambos os procedimentos, porém a decisão deve ser multidisciplinar e baseada principalmente na experiência da equipe
A manutenção da euvolemia e do volume circulante efetivo é recomendada, com a intenção de prevenir o surgimento de isquemia cerebral tardia
Hipervolemia profilática com a intenção de prevenir vasoespasmo não é recomendada
Ácido Tranexâmico pode ser uma opção nas primeiras 48h, em pacientes que não foram submetidos a correção do aneurisma, a fim de reduzir o risco de ressangramento precoce. Após 48 horas, aumenta o risco de isquemia cerebral, ou seja, seu uso é recomendado já com a certeza de que o aneurisma será clipado/embolizado dentro desse tempo. A dose é 1g 8/8h.
Não existe evidência para recomendação de anticonvulsivantes profiláticos
Pacientes comatosos devem ser mantidos com eletroencefalograma contínuo, para pesquisa de estado de mal epiléptico não convulsivo
Fenitoína é recomendada quando há crise convulsiva. Na ausência de crise convulsiva, pode-se administrar Fenitoína profilática, porém, por apenas 5 a 7 dias.
O uso de Dexametasona não é recomendado
Deve-se manter o paciente normotérmico
Até 50% dos pacientes podem apresentar hipertermia secundária a HSA. Hipotermia induzida só está indicada em casos de hipertensão intracraniana refratária.
De forma alguma deixar fazer febre. Para cada aumento de 1°C, o metabolismo cerebral aumenta de 6 a 8% e está associado a aumento da mortalidade. Dessa maneira, devemos deixar antipiréticos de horário e não ‘’à critério médico’’.
Recomenda-se fazer profilaxia para TEV com métodos mecânicos até que o aneurisma seja tratado
Uma nova recomendação é a dieta oral laxativa. Constipação pode aumentar a pressão intracraniana.
Durante a internação, deve-se realizar exame neurológico (Neurocheck) sumário a cada 1 a 4 horas, como também manter aferição contínua dos sinais vitais. O Neurocheck consiste em Escala de Coma de Glasgow, avaliação das pupilas, ritmo respiratório e déficits neurológicos.
Vasoespasmo e Isquemia Cerebral Tardia
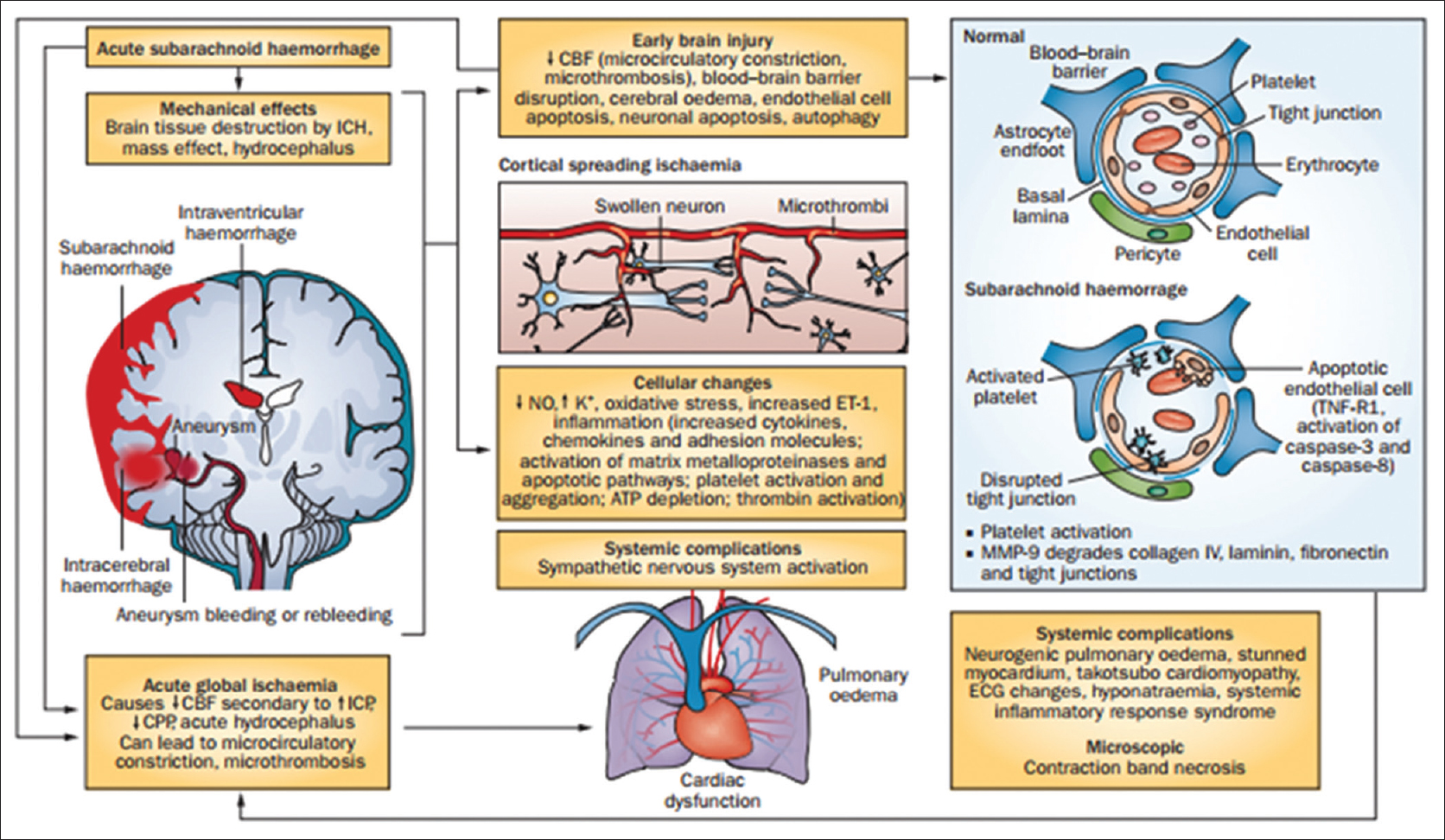
O vasoespasmo arterial se desenvolve do 4° ao 14° dia e tende a apresentar resolução após 21 dias
A fisiopatologia do vasoespasmo é ampla e esseocorre devido ao contato da Oxihemoglobina com a parede externa do vaso, lesão endotelial com liberação de Endotelina-1, NO, aumento de Glutamato e diversos outros fatores que discutiremos em uma outra postagem. 66% dos pacientes apresentam vasoespasmo angiográfico (sintomático ou não)
A isquemia cerebral tardia está associada a vasoespasmo em somente 50% dos casos, ou seja, o vasoespasmo é um diagnóstico de imagem. O diagnóstico clínico é a isquemia cerebral tardia.
Ao mesmo tempo que existem pacientes com vasoespasmo grave de grandes artérias que não se tornam sintomáticos, existem pacientes com vasoespasmo leve que desenvolvem não só isquemia como infarto cerebral
Não existe, hoje em dia, nenhum método efetivo para prevenção de vasoespasmo
Deve-se realizar doppler transcraniano para monitorar o surgimento de vasoespasmo
O doppler deve ser realizado diariamente ou a cada 2 dias, a depender do risco do paciente
O tratamento deve se basear no manejo da isquemia cerebral tardia e não existe indicação de tratamento do vasoespasmo não sintomático
Isquemia cerebral tardia se manifesta como piora, surgimento de novos déficits neurológicos e/ou redução do nível de consciência
O tratamento da isquemia cerebral tardia inclui:
Otimização hemodinâmica => Manter euvolemia e induzir Hipertensão (1 H)
Manter euvolemia é preferível do que hipervolemia
Hemodiluição também não é mais recomendada.
Se o aneurisma estiver tratado, deve-se aumentar a PA guiando-se pela resposta neurológica
Não induzir hipertensão se o paciente já estiver com PA elevada ou o status cardiovascular não permitir. Nesse caso deve-se preferir tratamento endovascular
As drogas vasoativas que podem ser usadas são noradrenalina, dopamina e fenilefrina, com preferência a noradrenalina
Se os sintomas neurológicos não apresentarem melhora com otimização hemodinâmica, existem duas opções terapêuticas:
Angioplastia com balão para lesões acessíveis (vasos proximais)
Vasodilatadores arteriais para lesões não acessíveis (bloqueadores do canal de cálcio ou óxido nítrico)
Outra complicações
Crises epilépticas são relatadas em 25% dos pacientes, sendo 20% delas não convulsivas e ocorrem mais comumente nas primeiras 24 horas
Ressangramento ocorre em até 15% dos casos nas primeiras 24 horas, tendo maior risco nas primeiras 12 horas
Hidrocefalia pode ocorrer em 15 a 85% dos pacientes e deve ser tratada com DVE ou drenagem lombar, a depender do cenário clínico, e ocorre por obstrução mecânica dos ventrículos pelo sangue.
Edema pulmonar cardiogênico ou neurogênico ocorre em 25% dos pacientes devido a descarga adrenérgica.
Arritmias cardíacas em 35% dos pacientes
No ECG, pode-se observar alterações da onda T, devido a disfunção autonômica intensa. As “ondas T cerebrais” são ondas T gigantes, negativas e difusas, em geral acompanhadas de desnivelamento de ST e aumento do intervato QT.
Hiponatremia em 10 a 30% dos pacientes. O controle do sódio é um dos principais pilares do tratamento da HSA. Recomenda-se manter o Na+ entre 145-150 meq/L. Além disso, não é recomendado administrar soluções hipotônicas (soro glicosado) pelo risco de hiponatremia e piora do edema cerebral.
Sempre atentar para Diabetes Insipidus, Síndrome Perdedora de Sal e SIADH
TVP pode ocorrer, principalmente, nos pacientes imobilizados
Até 46% dos pacientes que sobrevivem apresentam déficit cognitivo a longo prazo, com prejuízo a funcionalidade e qualidade de vida
Conclusões
A Hemorragia Subaracnoidea Aneurismática, além da alta mortalidade, tem impacto econômico significativo, pois atinge majoritariamente a população com idade produtivo e requer tratamento definitivo (clipagem/embolização) o mais rápido possível (de preferência, dentro das primeiras 48 horas).
Referências
Stroke. 2012;40
Kassel et al. J Neurosurgery 1990;73:18-47
Neurology 52:1602,1999
Stroke. 2001; 32: 2012-2020
Claassen J et al. Crit Care Med 2004;32:832-838
Neurology 2007;68:1013-1019
Curr Opinion Crit Care 2008;14:156
Dankbaar et al. critical care forum 2010,14:R23 Chugh C, Agarwal H. Cerebral vasospasm and delayed cerebral ischemia: Review of literature and the management approach. Neurol India [serial online] 2019 [cited 2020 Sep 14];67:185-200. Available from: http://www.neurologyindia.com/text.asp?2019/67/1/185/253627